Content
Tot i que tots els àtoms del mateix element contenen el mateix nombre de protons, el nombre de neutrons pot variar. Saber quants neutrons té un àtom determinat us pot ajudar a determinar si la partícula és regular en aquell element o un isòtop, que tindrà més o menys neutrons. Determinar el nombre de neutrons en un àtom és bastant senzill i no requereix cap experiment. Per calcular el nombre de neutrons en un àtom o isòtop regular, seguiu aquestes instruccions amb una taula periòdica a la mà.
Passos
Mètode 1 de 2: Trobar el nombre de neutrals en un àtom comú
Localitza l'element a la taula periòdica. Per aquest exemple, mirem el sistema operatiu (Os), que es troba a la sisena fila, de dalt a baix.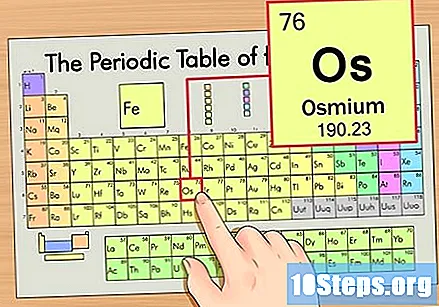
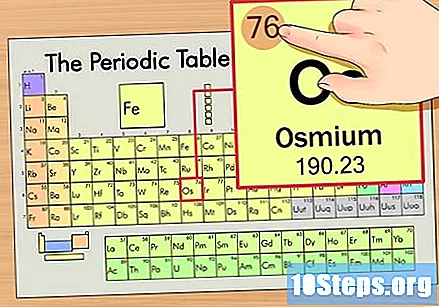
Trobeu el nombre atòmic de l’element. Aquest és normalment el nombre més visible d’un determinat element i sol estar per sobre del seu símbol (a la taula que estem utilitzant, de fet, no hi ha cap altre número enumerat). El nombre atòmic és el nombre de protons en un sol àtom d'aquest element. El nombre d’Os és de 76, el que significa que un àtom d’osmium té 76 protons.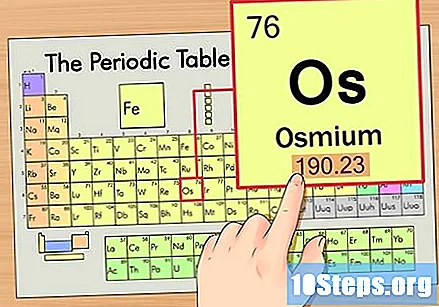
Troba el pes atòmic de l’element. Aquest nombre es troba normalment sota el símbol atòmic. Tingueu en compte que la taula d'aquest exemple només es basa en el nombre atòmic i no llista el pes atòmic. No sempre serà així. L’osmium té un pes atòmic de 190,23.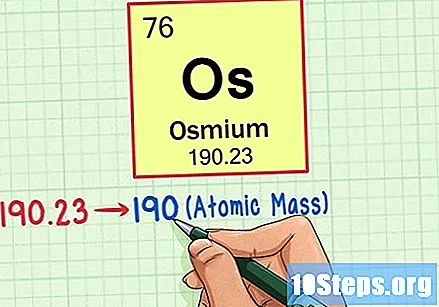
Arrodoneix el pes atòmic al nombre sencer més proper per trobar la massa atòmica. En el nostre exemple, el 190.23 s’arrodoniria fins al 190, resultant en una massa atòmica de 190 per a Osmium.- La massa atòmica és una mitjana dels isòtops de l’element. Per tant, no sol ser un nombre enter.
Resteu el nombre atòmic de la massa atòmica. Com que la gran majoria de la massa d’un àtom es troba en els seus protons i neutres, restant el nombre de protons (és a dir, el nombre atòmic) de la massa atòmica li donarà el nombre calculat de neutrons a l’àtom. El nombre després del punt decimal generalment representa una massa molt petita d’electrons a l’àtom. En el nostre exemple, es tracta de: 190 (massa atòmica) - 76 (nombre de protons) = 114 (nombre de neutrons).
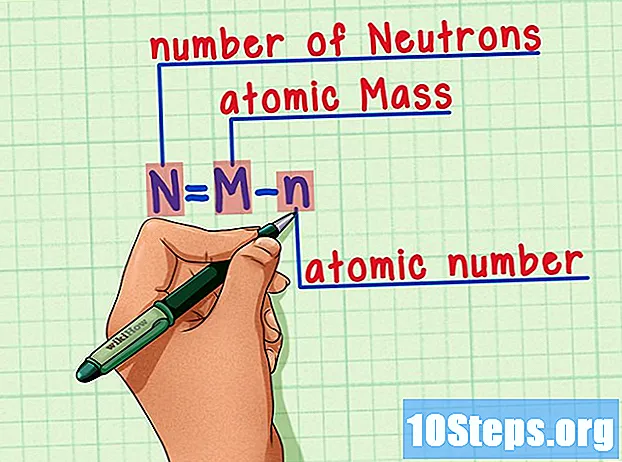
Recordeu la fórmula. Per trobar el nombre de neutrons en el futur, només cal que utilitzeu aquesta fórmula: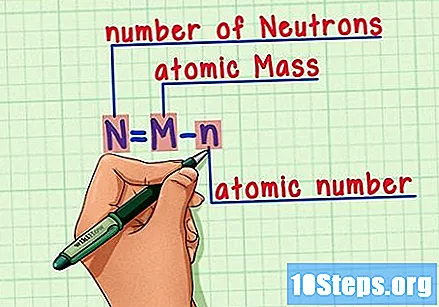
- N = M - n.
- N = nombre de Neutrons.
- M = Mrostit atòmic
- n = nhumerus atòmic.
- N = M - n.
Mètode 2 de 2: Trobar el nombre de neutrons en un isòtop
Localitza l'element a la taula periòdica. Per exemple, utilitzem l’isòtop carboni-14. Com que la forma no isotòpica de carboni-14 és simplement Carboni (C), trobeu aquest element a la taula periòdica (a la segona fila).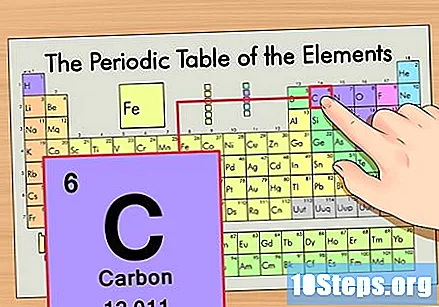
Trobeu el nombre atòmic de l’element. Aquest és normalment el nombre més visible d’un determinat element i sol estar per sobre del seu símbol (a la taula que estem utilitzant, de fet, no hi ha cap altre número enumerat). El nombre atòmic és el nombre de protons en un sol àtom d'aquest element. C és el número 6, el que significa que un àtom de carboni té 6 protons.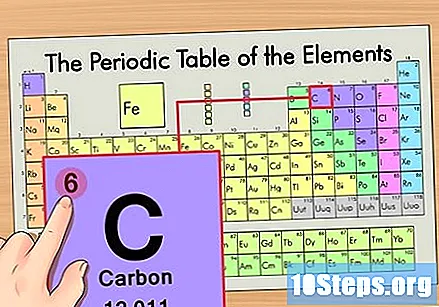
Troba la massa atòmica. Això és increïblement fàcil amb els isòtops, ja que reben el nom de la seva massa atòmica. El carboni-14 té una massa atòmica de 14. Un cop trobeu la massa atòmica de l’isòtop, el procés per trobar el nombre de neutrons és el mateix que es fa servir per als àtoms ordinaris.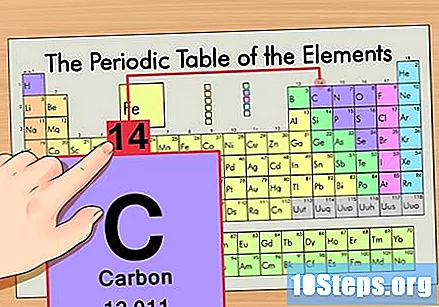
Resteu el nombre atòmic de la massa atòmica. Com que la gran majoria de la massa d’un àtom es troba en els seus protons i neutres, restant el nombre de protons (és a dir, el nombre atòmic) de la massa atòmica li donarà el nombre calculat de neutrons a l’àtom. El nombre després del punt decimal generalment representa una massa molt petita d’electrons a l’àtom. En el nostre exemple, es tracta de: 14 (massa atòmica) - 6 (nombre de protons) = 8 (nombre de neutrons).
Recordeu la fórmula. Per trobar el nombre de neutrons en el futur, només cal que utilitzeu aquesta fórmula: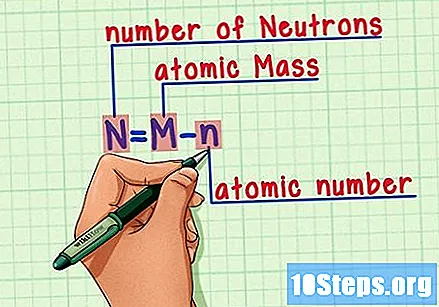
- N = M - n.
- N = nombre de Neutrons.
- M = Mrostit atòmic
- n = nhumerus atòmic.
- N = M - n.
Consells
- Osmium, un metall sòlid a temperatura ambient, deriva el seu nom de la paraula grega per "olor", "osme".
- Els protons i els neutrons constitueixen gairebé tot el pes dels elements, mentre que els electrons i altres partícules diverses representen una massa menyspreable (que s'aproxima a la massa zero). Com que un protó té el mateix pes que un neutre i el nombre atòmic representa el nombre de protons, podem restar el nombre de protons a la massa total.
- Si no esteu segurs de quin número es troba a la taula periòdica, només recordeu que normalment es fa al voltant del nombre atòmic (és a dir, el nombre de protons), que comença amb 1 (hidrogen) i puja una unitat per d’esquerra a dreta, finalitzant el 118 (Ununóctio). Això es deu al fet que el nombre de protons en un àtom determina què és aquest àtom, facilitant l’organització de la característica elemental (per exemple, un àtom amb 2 protons sempre serà Heli, de la mateixa manera que un altre àtom amb 79 protons serà sempre d’or).