Content
- etapes
- Mètode 1 Equilibrament d'una equació pel mètode d'assaig i error
- Mètode 2 Equilibra una equació pel mètode algebraic
En química, una equació estableix el que va passar durant una reacció química. A l’esquerra de l’equació, situem els reactius que s’utilitzaven per a l’experiment i a la dreta, els productes obtinguts durant l’experiment. Segons el principi de conservació de la massa (Lavoisier) durant una reacció química, no desapareix cap àtom, no es crea cap, es combinen de manera diferent. En resum, heu de tenir el mateix número de datomes de cada element a la dreta que a l’esquerra de l’equació. Per això, sempre s’ha d’equilibrar una equació d’equilibri.
etapes
Mètode 1 Equilibrament d'una equació pel mètode d'assaig i error
-
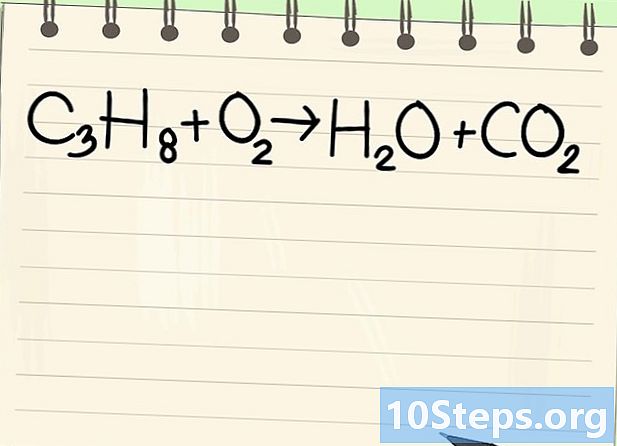
Tingueu en compte l’equació del saldo. Tractarem l’equació següent:- C3H8 + O2 -> H2O + CO2
- Aquesta és l’equació de la combustió del propà (C3H8) en oxigen: s’obté aigua i diòxid de carboni.
-
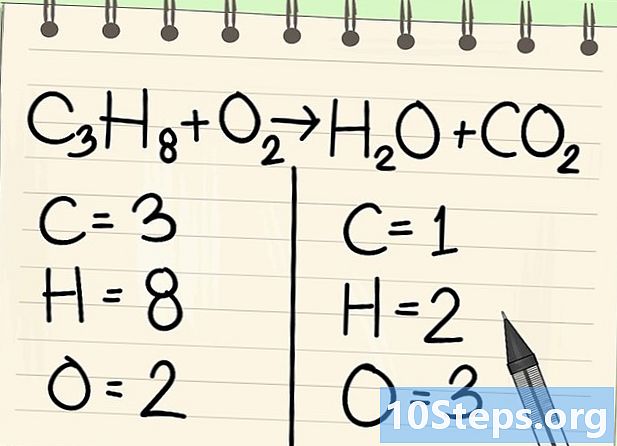
Comptar els àtoms. Introduïu el nombre de bases de dades de cada element en un costat de l'equació i, a continuació, en l'altre. Per això, tingueu en compte els índexs, si no n'hi ha, l'índex és 1.- A l'esquerra hi ha 3 àtoms de carboni, 8 d'hidrogen i 2 d'oxigen.
- A la dreta, hi ha 1 àtom de carboni, 2 d'hidrogen i 3 d'oxigen.
-
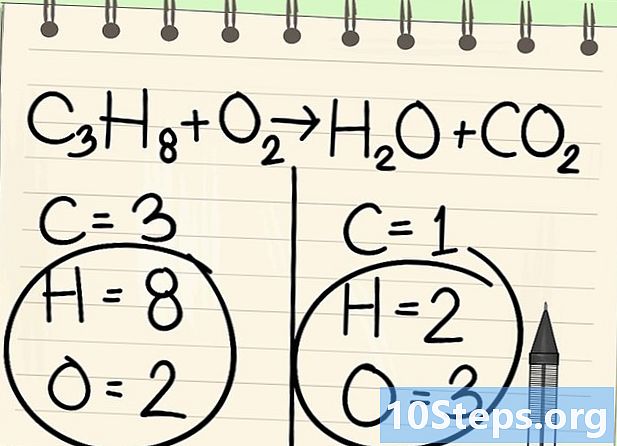
Deixeu de banda momentàniament l’hidrogen i l’oxigen. -

Comença a equilibrar amb l’element adequat. Sempre comencem amb la d’una molècula abans i després de la reacció. Si n’hi ha diversos, agafeu el que és monovalent en una de les molècules. Aquí comencem amb els àtoms de carboni. -

Equilibra els àtoms de carboni. Afegiu, a la dreta, un coeficient a la molècula de diòxid de carboni (CO)2) en què el latome de carboni està sol. Posarem un 3 per obtenir els 3 àtoms que queden.- C3H8 + O2 -> H2O + 3Colorado2
- Així tenim 3 àtoms de carboni a la dreta gràcies al coeficient (3CO)2) i 3 àtoms de carboni a l’esquerra gràcies a l’índex (C3H8).
- En una equació, podeu posar tots els coeficients que vulgueu, però no podeu tocar les pistes.
-
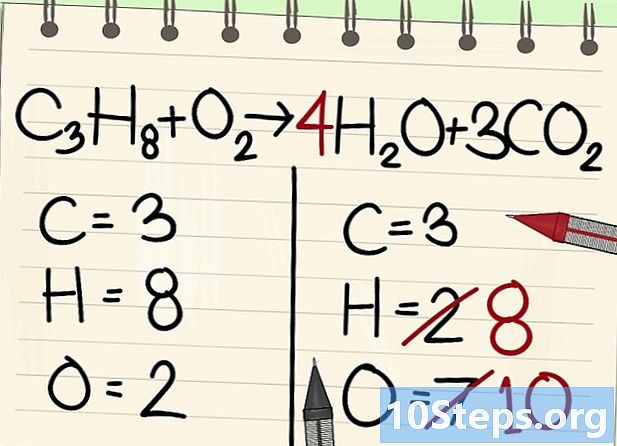
Equilibra els àtoms d'hidrogen. Com que teniu a l'esquerra de l'equació, necessiteu la mà dreta.- C3H8 + O2 --> 4H2O + 3CO2
- A la dreta, hi posareu un coeficient de 4, perquè l’hidrogen és bivalent a la molècula d’aigua: l’índex 2 indica que hi ha associats dos àtoms d’hidrogen.
- Per obtenir el nombre d’àtoms d’hidrogen a la dreta, multipliqueu el coeficient 4 per l’índex 2 o 8 àtoms.
- Pel que fa als àtoms d’oxigen, a la dreta, ara n’hi ha 6 d’un costat, procedents de les tres molècules de 3CO2 (3 x 2 = 6 àtoms) i 4 de les 4 molècules de 4 H2O (4 x 1 = 4 àtoms), és a dir, un total de 10 àtoms d'oxigen.
-
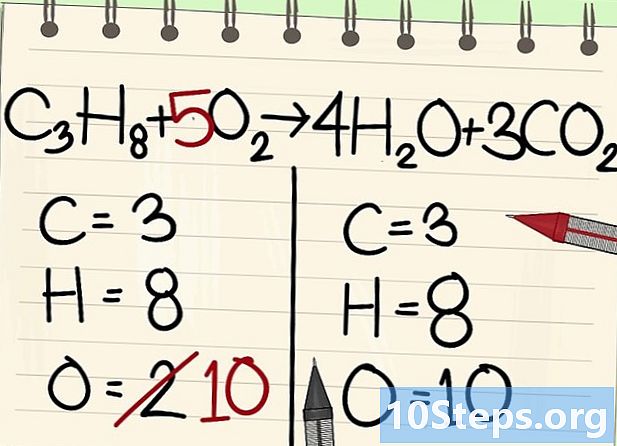
Equilibra els àtoms de l’oxigen.- A causa del balanç de carboni i hidrogen, el nombre d'àtoms d'oxigen no és el mateix a banda i banda de l'equació. Abans vam veure que hi havia 10 àtoms d’oxigen a la dreta (4 de molècules d’aigua i 6 de molècules de diòxid de carboni). A l'esquerra, només hi ha 2 (de l'O2).
- Per equilibrar l’oxigen, afegiu un coeficient de 5 a la molècula d’oxigen esquerra: teniu 10 àtoms d’oxigen a l’esquerra i l’altre a la dreta.
- C3H8 + 5O2 -> 4H2O + 3CO2
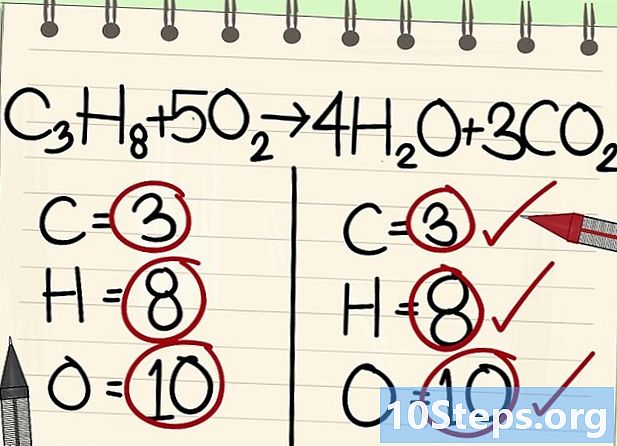
- Tots els àtoms (carboni, hidrogen i oxigen) són equilibrats: la vostra equació és equilibrada.
Mètode 2 Equilibra una equació pel mètode algebraic
-

Escriu l’equació a l’equilibri. Assigna a cada molècula un coeficient literal. Els anomenarem té, b, c i d. -
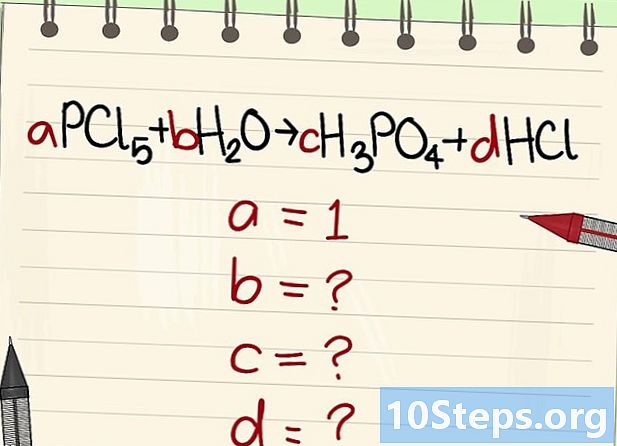
Cerqueu el valor dels altres coeficients literals. Això ho demanarem té = 1. -

Trobeu les relacions entre aquests coeficients. Mirant a l’esquerra (reactius) i a la dreta (productes), estableix les relacions entre aquests diferents coeficients.- Preneu l’equació següent: aPCl5 + bH2O = cH3PO4 + dHCl. S'ha afirmat que a = 1, el que significa que c = a, d = 5a i 2b = 3c + d. Càlculs fets, c = 1, d = 5 i b = 4.

- Preneu l’equació següent: aPCl5 + bH2O = cH3PO4 + dHCl. S'ha afirmat que a = 1, el que significa que c = a, d = 5a i 2b = 3c + d. Càlculs fets, c = 1, d = 5 i b = 4.